發(fÄ)布日期:2025-01-06 ç€è¦½æ¬¡æ•¸(shù):110
2025å¹´1月3日,由浙江çœè…«ç˜¤é†«(yÄ«)院范云教授團(tuán)隊(duì)牽é é–‹å±•çš„ä¸€é …(xià ng)å¡ç‘žåˆ©ç 單抗è¯(lián)åˆè…¦éƒ¨æ”¾ç™‚åŠå«é‰‘雙藥化療治療åˆæ²»æ™šæœŸéžå°ç´°(xì)胞肺癌åˆå¹¶è…¦è½‰(zhuÇŽn)移患者的多ä¸å¿ƒã€å–®è‡‚çš„â…¡æœŸè‡¨åºŠç ”ç©¶(C-Brain)于國(guó)際腫瘤å¸(xué)é ˜(lÇng)åŸŸé ‚ç´š(jÃ)期刊《柳葉刀·腫瘤å¸(xué)》《The Lancet Oncology》(IF:41.6)1在線發(fÄ)表。
C-Brainç ”ç©¶æ˜¯å…¨çƒé¦–個(gè)將放療與å…疫和化療è¯(lián)åˆæ‡‰(yÄ«ng)用于晚期驅(qÅ«)å‹•(dòng)åŸºå› é™°æ€§éžå°ç´°(xì)胞肺癌(NSCLC)腦轉(zhuÇŽn)移患者的å‰çž»æ€§ç ”究,首次探索了å¡ç‘žåˆ©ç 單抗è¯(lián)åˆåŒ–療åŠå±€éƒ¨æ”¾ç™‚在NSCLC腦轉(zhuÇŽn)移患者ä¸çš„療效和安全性,有望為æ¤é¡žæ‚£è€…æ供全新的治療é¸æ“‡ã€‚
èŒƒäº‘æ•™æŽˆé ˜(lÇng)銜C-BRAINç ”ç©¶ç™¼(fÄ)布于The Lancet Oncology
01 ç ”ç©¶èƒŒæ™¯
腦轉(zhuÇŽn)移與NSCLCçš„ä¸è‰¯é (yù)åŽå¯†åˆ‡ç›¸é—œ(guÄn)ï¼›20-30%çš„NSCLC患者在åˆæ¬¡è¨ºæ–·æ™‚(shÃ)åˆå¹¶è…¦è½‰(zhuÇŽn)移,顯著影響患者的生å˜å’Œç”Ÿæ´»è³ª(zhì)é‡2,3。由于化療藥物ä¸èƒ½æœ‰æ•ˆç©¿é€è¡€è…¦å±éšœï¼Œæ‰‹è¡“(shù)切除åŠæ”¾ç™‚是NSCLC腦轉(zhuÇŽn)移綜åˆæ²»ç™‚ä¸çš„é‡è¦æ‰‹æ®µï¼Œä½†ç™‚æ•ˆæ¬ ä½³ã€‚é‡å°(duì)é€™ä¸€æœªæ»¿è¶³éœ€æ±‚ï¼Œç ”ç©¶è€…å‰æœŸé–‹å±•äº†PD-1/PD-L1單抗單藥或者è¯(lián)åˆåŒ–療治療NSCLC腦轉(zhuÇŽn)移患者的å°æ¨£æœ¬ã€å‰çž»æ€§ç ”究,ç´å…¥äººç¾¤ä¸»è¦ç‚ºç„¡ç™¥ç‹€ã€å°ç—…ç¶æ‚£è€…群體。然而在臨床實(shÃ)è¸ä¸ï¼Œæœ‰ç™¥ç‹€æˆ–ç—…ç¶è¼ƒå¤§çš„腦轉(zhuÇŽn)移患者常常需è¦è¯(lián)åˆè…¦éƒ¨æ”¾ç™‚ã€‚æ—¢å¾€ç ”ç©¶æ示,腦部放療è¯(lián)åˆå…疫治療具有å”(xié)åŒæŠ—腫瘤活性,似乎是伴腦轉(zhuÇŽn)移NSCLC患者的一種潛在治療手段4。但目å‰ç›¸é—œ(guÄn)ç ”ç©¶é–‹å±•è¼ƒå°‘ï¼Œä»ç¼ºä¹è¼ƒç‚ºæ˜Žç¢ºçš„應(yÄ«ng)用è‰æ“š(jù)ã€‚å› æ¤ï¼Œå¦‚何有效治療腦轉(zhuÇŽn)移患者是臨床醫(yÄ«)ç”Ÿå¿…é ˆè€ƒæ…®çš„å•é¡Œã€‚
å¡ç‘žåˆ©ç 單抗是æ’瑞醫(yÄ«)è—¥è‡ªä¸»ç ”ç™¼(fÄ)的一種人æºåŒ–IgG4單克隆抗體,其è¯(lián)åˆé‰‘類雙藥化療已在ä¸åœ‹(guó)ç²æ‰¹ç”¨äºŽæ™šæœŸNSCLC患者的一線治療5,6。2023年,Ⅱ期CAP-BRAINç ”ç©¶é¡¯ç¤ºäº†å¡ç‘žåˆ©ç 單抗è¯(lián)åˆæ²»ç™‚方案作為晚期éžé±—ç‹€NSCLC伴腦轉(zhuÇŽn)移患者一線治療的潛力7ã€‚æœ¬é …(xià ng)â…¡æœŸç ”ç©¶ï¼Œæ—¨åœ¨ç ”ç©¶å¡ç‘žåˆ©ç 單抗è¯(lián)åˆè…¦æ”¾ç™‚和鉑類雙藥化療在未經(jÄ«ng)治療的晚期éžé±—狀和鱗狀NSCLC伴腦轉(zhuÇŽn)移患者ä¸çš„療效和安全性。
02 ç ”ç©¶æ–¹æ³•
2020å¹´5月6日至2023å¹´1月30日,共ç´å…¥65例NSCLCåˆå¹¶è…¦è½‰(zhuÇŽn)移患者接å—了å¡ç‘žåˆ©ç 單抗è¯(lián)åˆè…¦éƒ¨æ”¾ç™‚åŠå«é‰‘雙藥治療。主è¦ç ”究終點(diÇŽn)為6個(gè)月無進(jìn)展生å˜(PFS)率。次è¦çµ‚點(diÇŽn)包括RECIST v1.1定義PFSã€é¡±å…§(nèi)PFS(iPFS)ã€ç¸½é«”客觀緩解率(ORR)ã€é¡±å…§(nèi)客觀緩解率(iORR)ã€ç–¾ç—…控制率(DCR)ã€ç¸½ç”Ÿå˜æœŸ(OS)和安全性。

圖1. ç ”ç©¶è¨(shè)計(jì)
ç ”ç©¶ç´å…¥å½±åƒå¸(xué)診斷的NSCLC腦轉(zhuÇŽn)移(≥5 mm)患者,å°(duì)腦轉(zhuÇŽn)移病ç¶çš„最大直徑ã€æ•¸(shù)é‡åŠä¸æ¨žç¥žç¶“(jÄ«ng)系統(tÇ’ng)癥狀沒有é™åˆ¶ï¼Œæ ¹æ“š(jù)RECIST v1.1標(biÄo)準(zhÇ”n)至少有å¯æ¸¬(cè)é‡çš„é¶ç—…ç¶ï¼Œç„¡EGFR/ALK/ROS1çªè®Šï¼ŒECOG PS為0或1分,é (yù)期壽命≥3個(gè)月。
患者按腦部病ç¶æ•¸(shù)é‡æŽ¥å—ä¸åŒå±€éƒ¨æ²»ç™‚方案:腦轉(zhuÇŽn)移ç¶(BMs)為1~4個(gè)的患者原則上接å—立體定å‘放射外科(SRS)20-35 Gy,1~5分次;BMs≥5個(gè)的患者原則上接å—全腦放射治療(WBRT)3.0 Gy*10分次。在開始SRS或WBRTçš„7天內(nèi)進(jìn)è¡Œå¡ç‘žåˆ©ç 單抗200 mg Q3w,在å¡ç‘žåˆ©ç 單抗治療第1個(gè)或第2個(gè)療程è¯(lián)åˆå«é‰‘雙藥化療。
03 ç ”ç©¶çµ(jié)æžœ
ç ”ç©¶å…±å…¥çµ„äº†65例患者,46例(71%)患者在入組時(shÃ)有癥狀性腦轉(zhuÇŽn)移。截至2023å¹´12月13日,ä¸ä½éš¨è¨ªæ™‚(shÃ)間為14.1個(gè)月,19例(29%)患者ä»åœ¨æŽ¥å—å¡ç‘žåˆ©ç 單抗ç¶æŒæ²»ç™‚。65例患者ä¸æœ‰39例(60%)接å—了SRS治療,24例(37%) 患者接å—總劑é‡ç‚º30 Gy(æ¯æ¬¡3 Gy)çš„WBRT。å¡ç‘žåˆ©ç 單抗的ä¸ä½æ²»ç™‚周期數(shù)為7(IQR:4-11),鉑類雙藥化療的ä¸ä½æ²»ç™‚周期數(shù)為4(IQR:3-4)。從腦部放療到å…疫治療的ä¸ä½æ™‚(shÃ)間間隔為2天(IQR:1-6)。
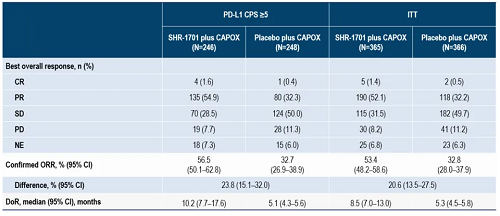
1.臨床療效
在全分æžé›†(FAS)ä¸ï¼Œä¸»è¦çµ‚點(diÇŽn)6個(gè)月PFS率為71.7%(95% CI:58.9%-81.1%),ä¸ä½PFS為10.7個(gè)月(95% CI:7.5-15.7),ä¸ä½iPFS為16.1個(gè)月(95% CI:13.0-NR),ä¸ä½OS為20.9個(gè)月(95% CI:13.8-27.7)。
圖2:PFS(A)ã€iPFS(B)åŠOS(C)çš„Kaplan-Meier曲線
(ä¾æ“š(jù)RECIST 1.1標(biÄo)準(zhÇ”n))
在FASä¸ï¼ŒiORR為78.5%(95% CI:66.5%-87.7%),顱內(nèi)疾病控制率(iDCR)為98.5%(95% CI:91.7%-100%),顱外病ç¶çš„ORR為69.2%(95% CI:56.6%-80.1%),DCR為93.8%(95% CI:85.0%-98.3%)ï¼›
å°(duì)于å¯è©•(pÃng)ä¼°ä¸æ¨žç¥žç¶“(jÄ«ng)系統(tÇ’ng)ç—…ç¶ç™‚效(cEFR)的患者,iORR為82.5%(95% CI:70.1%-91.3%),iDCR為98.2%(95% CI:90.6%-100%),ORR為70.2%(95% CI:56.6%-81.6%),DCR為96.5%(95% CI:87.9%-99.6%)。

表1. 顱內(nèi)和全身腫瘤緩解
腦部é¶ç—…ç¶çš„最佳百分比變化ä¸ä½å€¼ç‚º68.3%(IQR:38.8%-100.0%)。全身緩解ä¸ä½æ™‚(shÃ)間為1.8個(gè)月(95% CI:1.5-2.2),全身緩解的ä¸ä½æŒçºŒ(xù)時(shÃ)間為9.5個(gè)月(95% CI:6.1-14.6)。整體é¶ç—…ç¶çš„最佳百分比變化ä¸ä½å€¼ç‚º46.9%(IQR:30.3-67.7)。

圖3. cEFRä¸é¡±å…§(nèi)或整體é¶ç—…ç¶ç›´å¾‘總和與基線相比的最佳百分比變化
(A.æ¢å½¢é¡è‰²è¡¨ç¤ºæ ¹æ“š(jù)RECIST 1.1的最佳顱內(nèi)或全身å應(yÄ«ng)。*表示顱內(nèi)或全身é¶ç—…ç¶ç›´å¾‘總和與基線相比無變化[0%]的患者;B.顯示FAS隊(duì)列顱內(nèi)和整體é¶ç—…變的å應(yÄ«ng)時(shÃ)é–“å’Œå應(yÄ«ng)æŒçºŒ(xù)時(shÃ)é–“)
2.安全性
å¡ç‘žåˆ©ç 單抗è¯(lián)åˆè…¦éƒ¨æ”¾ç™‚åŠå«é‰‘雙藥化療治療åˆæ²»æ™šæœŸéžå°ç´°(xì)胞肺癌åˆå¹¶è…¦è½‰(zhuÇŽn)移患者安全性整體å¯æŽ§ã€‚
04 ç ”ç©¶çµ(jié)è«–
å¡ç‘žåˆ©ç 單抗è¯(lián)åˆè…¦éƒ¨æ”¾ç™‚åŠå«é‰‘雙藥化療顯示出良好的療效和å¯æŽ§çš„安全性,有望為éžå°ç´°(xì)胞肺癌腦轉(zhuÇŽn)移患者æ供全新的治療é¸æ“‡ã€‚åŒæ™‚(shÃ)期待åŽçºŒ(xù)進(jìn)一æ¥é–‹å±•éš¨æ©Ÿ(jÄ«)å°(duì)照試驗(yà n)。
åƒè€ƒæ–‡ç»(xià n):
[1].Xu, Yanjun et al. Brain radiotherapy combined with camrelizumab and platinum-doublet chemotherapy for previously untreated advanced non-small-cell lung cancer with brain metastases (C-Brain): a multicentre, single-arm, phase 2 trial. The Lancet Oncology, Volume 26, Issue 1, 74 – 84.
[2].Cagney DN, Martin AM, Catalano PJ, et al. Incidence and prognosis of patients with brain metastases at diagnosis of systemic malignancy: a population-based study. Neuro Oncol. 2017;19(11):1511-21.
[3].Gillespie CS, Mustafa MA, Richardson GE, et al. Genomic Alterations and the Incidence of Brain Metastases in Advanced and Metastatic NSCLC: A Systematic Review and Meta-Analysis. J Thorac Oncol. 2023;18(12):1703-13.
[4].Yang Yin, Deng Lei, Yang Yufan, et al. Efficacy and Safety of Combined Brain Radiotherapy and Immunotherapy in Non-Small-Cell Lung Cancer With Brain Metastases: A Systematic Review and Meta-Analysis.[J] .Clin Lung Cancer, 2022, 23: 95-107.
[5].Zhou C, Chen G, Huang Y, et al. Camrelizumab plus carboplatin and pemetrexed versus chemotherapy alone in chemotherapy-naive patients with advanced non-squamous non-small-cell lung cancer (CameL): a randomised, open-label, multicentre, phase 3 trial. Lancet Respir Med 2021; 9: 305–14.
[6].Ren S, Chen J, Xu X, et al. Camrelizumab plus carboplatin and paclitaxel as first-line treatment for advanced squamous NSCLC (CameL-Sq): a phase 3 trial. J Thorac Oncol 2022; 17: 544–57.
[7].Hou X, Zhou C, Wu G, et al. Efficacy, safety, and health-related quality of life with camrelizumab plus pemetrexed and carboplatin as first-line treatment for advanced nonsquamous NSCLC with brain metastases (CAP-BRAIN): a multicenter, open-label, singlearm, phase 2 study. J Thorac Oncol 2023; 18: 769–79.








