發布日期:2024-12-31 ç€è¦½æ¬¡æ•¸ï¼š95
2024年第47屆圣安æ±å°¼å¥§ä¹³è…ºç™Œç ”討會(SABCS)于近日在美國圣安æ±å°¼å¥§èˆ‰è¡Œã€‚期間,由ä¸åœ‹é†«å¸ç§‘å¸é™¢è…«ç˜¤é†«é™¢é¦¬é£›æ•™æŽˆåœ˜éšŠç‰½é 的“é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚在HR+/HER2-晚期乳腺癌內臟å±è±¡æ‚£è€…ä¸çš„æŽ¢ç´¢æ€§ç ”ç©¶â€çš„最新çµæžœï¼ˆæ‘˜è¦è™Ÿç‚ºP2-09-28ï¼‰ç²¾å½©äº®ç›¸ã€‚è©²ç ”ç©¶é”到了é è¨çš„主è¦çµ‚點,æ示é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚有望æˆç‚ºæ¤é¡žæ‚£è€…çš„æ–°é¸æ“‡[1]。
01ç ”ç©¶èƒŒæ™¯
å°äºŽåˆå¹¶å…§è‡Ÿå±è±¡çš„晚期乳腺癌患者,目å‰è‡¨åºŠä¸Šä¸»è¦é¸æ“‡åŒ–療,以é”到快速控制疾病進展的目的[2]。然而,由于內臟å±è±¡æ‚£è€…通常伴器官功能障礙,臨床上很難é¸æ“‡åˆé©çš„化療方案。æ¤å¤–,內臟å±è±¡äººç¾¤å¸¸å¸¸è¢«æŽ’é™¤åœ¨ä¹³è…ºç™Œè‡¨åºŠè©¦é©—çš„ç ”ç©¶å°è±¡ä¹‹å¤–,導致內臟å±è±¡çš„治療ç–略缺ä¹å……分的å‰çž»æ€§ç ”究è‰æ“šã€‚å› æ¤ï¼Œè¿«åˆ‡éœ€è¦æ–°çš„治療é¸æ“‡ä¾†æ”¹å–„這部分患者的é åŽã€‚
é”爾西利是æ’ç‘žé†«è—¥è‡ªä¸»ç ”ç™¼çš„1類新藥,也是ä¸åœ‹é¦–å€‹è‡ªä¸»ç ”ç™¼çš„æ–°åž‹é«˜é¸æ“‡æ€§CDK4/6抑制劑,于2021å¹´12月ç²åœ‹å®¶è—¥ç›£å±€æ‰¹æº–ä¸Šå¸‚ï¼Œå·²åœ¨ä¹³è…ºç™Œæ²»ç™‚é ˜åŸŸç²æ‰¹å…©å€‹é©æ‡‰ç™¥ã€‚
æœ¬ç ”ç©¶æ—¨åœ¨è©•ä¼°é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚å°æ¯”化療在HR+/HER2-晚期乳腺癌伴內臟å±è±¡æ‚£è€…ä¸çš„療效與安全性。
02 ç ”ç©¶æ–¹æ³•
æœ¬ç ”ç©¶ç‚ºä¸€é …å¤šä¸å¿ƒã€å¤–部å°ç…§çš„Ⅱ期臨床試驗,試驗組采用Simon兩階段è¨è¨ˆï¼Œæ—¨åœ¨è©•ä¼°é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚在HR+/HER2-晚期乳腺癌伴內臟å±è±¡æ‚£è€…ä¸çš„療效與安全性。
內臟å±è±¡å®šç¾©ï¼šèƒ¸è…”ç©æ¶²ï¼Œè…¹æ°´ï¼Œè‚臟或腹膜轉移引起的腹痛,胸腔ç©æ¶²æˆ–肺淋巴管炎引起的呼å¸å›°é›£ï¼Œè‚é…¶å‡é«˜ï¼ˆ>2×ULN),在無Gilbert綜åˆå¾æˆ–膽é“梗阻的情æ³ä¸‹ï¼Œè†½ç´…ç´ å¿«é€Ÿå‡é«˜ï¼ˆ>1.5×ULN),病ç†å¸è‰å¯¦çš„骨髓轉移且血紅蛋白<100 g/L。
æœ¬ç ”ç©¶ä¸ï¼Œè©¦é©—組å—試者將接å—é”爾西利(150mgæ¯æ—¥å£æœï¼Œå‰21天連續æœè—¥ï¼ŒåŽ7天åœè—¥ï¼‰è¯åˆç ”究者é¸æ“‡çš„內分泌治療(ETï¼‰æ–¹æ¡ˆã€‚åœ¨ç ”ç©¶ç¬¬ä¸€éšŽæ®µï¼Œå°‡å…¥çµ„18例å—試者,若觀察到的6個月å˜æ´»å—試者數≥9例,則進入第二階段并繼續入組35例å—試者。在總計53例å—試者ä¸ï¼Œè‹¥6個月å˜æ´»å—試者數≥28例,則表明該方案值得進一æ¥æŽ¢ç´¢ã€‚
æœ¬ç ”ç©¶ä½¿ç”¨çœŸå¯¦ä¸–ç•Œæ•¸æ“šä½œç‚ºå¤–éƒ¨å°ç…§çµ„,é¸å–接å—化療的HR+/HER2-晚期乳腺癌內臟å±è±¡æ‚£è€…(CT組)。這些數據來æºäºŽå„ä¸å¿ƒçš„醫院信æ¯ç³»çµ±ï¼ˆHIS)。CT組的入組標準和排除標準與é”爾西利+ET組相åŒã€‚é‡‡ç”¨é€†æ¦‚çŽ‡åŠ æ¬Šï¼ˆIPTW)方法來評估試驗組的平å‡æ²»ç™‚效應(ATT),并進行傾å‘評分調整,包括年齡ã€ECOG評分ã€å¾©ç™¼ã€è½‰ç§»éƒ¨ä½æ•¸é‡ã€æ—¢å¾€æ™šæœŸåŒ–療線數和內臟å±è±¡é¡žåˆ¥ã€‚
æœ¬ç ”ç©¶çš„ä¸»è¦çµ‚點為6個月總生å˜çŽ‡ï¼ˆ6個月OS)。次è¦çµ‚點包括:總生å˜æœŸï¼ˆOS)ã€ç„¡é€²å±•ç”Ÿå˜æœŸï¼ˆPFS)ã€å®¢è§€ç·©è§£çŽ‡ï¼ˆORR)ã€ç–¾ç—…控制率(DCR)ã€3個月治療失敗率(TFR)ã€è‡³æ²»ç™‚失敗時間(TTF)ã€ç–¾ç—…控制時間(DDC)以åŠä¸è‰¯äº‹ä»¶ï¼ˆAE)和嚴é‡ä¸è‰¯äº‹ä»¶ï¼ˆSAE)的發生率åŠåš´é‡ç¨‹åº¦ï¼ˆåœ–1)。
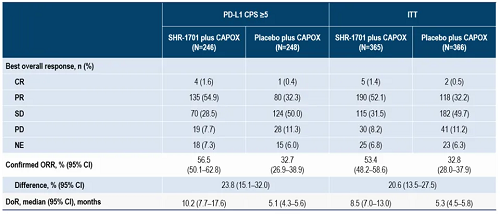
圖 1 ç ”ç©¶è¨è¨ˆåœ–
03 ç ”ç©¶çµæžœ
1.有效性çµå±€
在2023å¹´2月至2024å¹´9月期間,在第一階段試驗組18例患者ä¸ï¼Œæœ‰17例患者的生å˜è¶…éŽ6個月。在進入第二階段53例患者ä¸ï¼Œ49例患者的生å˜è¶…éŽ6個月,6個月生å˜çŽ‡é”到92.5%(95% CI,81.8-97.9),æˆåŠŸæ‹’絕了原å‡è¨ï¼ˆâ‰¤44%)。其ä¸11例(20.8%)é”到部分緩解(PR),31例(58.5%)é”到疾病穩定(SD),ORRé”到20.8%(95% CI,10.8-34.1),DCRé”到79.2%(95% CI,65.9-89.2)。3個月TFR為22.6%(95% CI,12.3-36.2)。
å°CT組的157例患者數據進行分æžã€‚經IPTW調整åŽï¼Œæœ‰æ•ˆæ¨£æœ¬é‡ç´„為50例(表1)。與CT組相比,é”爾西利+ET組的ä¸ä½PFS更長(ä¸ä½10.74個月 vs. 4.63個月;HR=0.316[95% CI,0.191-0.521],P<0.0001),ä¸ä½TTF也更長(ä¸ä½9.46個月 vs. 4.14個月;HR=0.301[95% CI,0.184-0.494],P<0.0001)。é”爾西利+ET組ä¸ä½DDC為10.68個月,CT組ä¸ä½DDC為5.03個月(圖2)。

表1 IPTW調整å‰åŽçš„基線特å¾
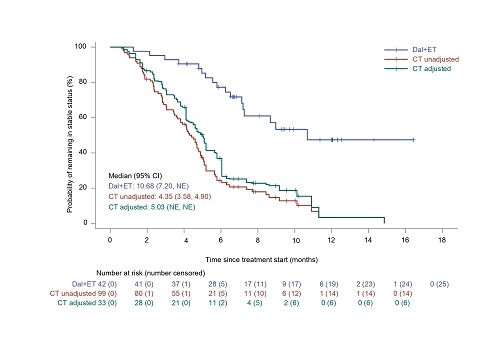


圖2 IPTW調整å‰åŽçš„PFSã€TTFå’ŒDDCçš„KM曲線
2.治療相關ä¸è‰¯å應
é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚安全性å¯æŽ§ï¼Œæœªè§€å¯Ÿåˆ°æ–°çš„安全性信號。
04 ç ”ç©¶ç¸½çµ
æœ¬ç ”ç©¶é”到了é è¨çš„主è¦çµ‚點,é”爾西利è¯åˆET組的6個月OS為92.5%。æ¤å¤–,與CT組相比,é”爾西利è¯åˆET組顯著延長了患者的PFSå’ŒTTF。é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚安全性å¯æŽ§ï¼Œæœªè§€å¯Ÿåˆ°æ–°çš„安全性信號,æ示é”爾西利è¯åˆå…§åˆ†æ³Œæ²»ç™‚有望æˆç‚ºHR+/HER2-晚期乳腺癌伴內臟å±è±¡æ‚£è€…的新治療é¸æ“‡ã€‚
åƒè€ƒæ–‡ç»ï¼š
[1] Hongnan M, et al. Dalpiciclib plus endocrine therapy for visceral crisis in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: a multicenter, phase 2 study. 2024 SABCS P2-09-28.
[2] Gennari A, et al. ESMO Clinical Practice Guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Ann Oncol, 2021. 32(12): 1475-1495.








