職位推薦
- 珍格醫(yī)療-臨床銷售 15001-20000
- 地奧制藥-醫(yī)藥代表 6001-8000
- 普利德醫(yī)療-醫(yī)療設(shè)備銷售經(jīng)理 面議
- 大唐-兼職招商經(jīng)理 面議
- 景德中藥-直營經(jīng)理 6001-8000
- 安邦醫(yī)藥-省區(qū)招商經(jīng)理 8001-10000
- 恒瑞醫(yī)藥-醫(yī)藥信息溝通專員 6001-8000
- 黃河中藥-學(xué)術(shù)講師 8001-10000
發(fā)布日期:2024-08-27 瀏覽次數(shù):101
近日,恒瑞醫(yī)藥子公司蘇州盛迪亞生物醫(yī)藥有限公司收到國家藥品監(jiān)督管理局核準(zhǔn)簽發(fā)的《藥品注冊證書》,批準(zhǔn)公司自主研發(fā)的1類新藥夫那奇珠單抗注射液(安達(dá)靜?)上市,用于治療適合接受系統(tǒng)治療或光療的中重度斑塊狀銀屑病成人患者。該產(chǎn)品是公司在自身免疫疾病領(lǐng)域上市的首個創(chuàng)新藥,也是中國首個獲批的本土自主研發(fā)重組抗IL-17A人源化單克隆抗體,將打破同類進口藥物的長期壟斷局面,為銀屑病患者提供新的治療選擇。至此,恒瑞醫(yī)藥獲批上市的創(chuàng)新藥達(dá)17款。
銀屑病是一種自身免疫性皮膚病,目前無法根治,其負(fù)面影響程度與疾病嚴(yán)重程度密切相關(guān)。據(jù)統(tǒng)計,我國銀屑病患者約700多萬,其中中重度銀屑病患者占比高達(dá)57.3%,估算有近400萬人1-3。目前臨床亟需皮損清除率高、起效快、療效持久且安全性高的治療新手段。
生物制劑靶向IL-17A治療銀屑病,在理論上能夠快速起效的機制優(yōu)勢,已得到大量臨床數(shù)據(jù)的充分證實4-6。夫那奇珠單抗是人源化抗體,具有0.8%鼠源成分,保留了來自鼠源的6個CDR區(qū),同時具有“創(chuàng)新結(jié)合表位”,從而保證了對IL-17A的高親和力,能實現(xiàn)與IL-17A精準(zhǔn)結(jié)合,高效靶向阻斷IL-17A通路;同時較低的鼠源成分,也降低了潛在的免疫原性7。
此次夫那奇珠單抗獲批上市是基于一項在全國開展的多中心、隨機、雙盲、平行、安慰劑對照的臨床 III 期研究(SHR-1314-301)8,研究表明,與安慰劑相比,夫那奇珠單抗對中重度斑塊狀銀屑病具有統(tǒng)計學(xué)顯著性和臨床意義的改善。同時,夫那奇珠單抗在中重度慢性斑塊狀銀屑病患者中長期治療的安全性、耐受性良好。
作為創(chuàng)新型國際化制藥企業(yè),恒瑞醫(yī)藥多年來持續(xù)圍繞臨床急需進行創(chuàng)新研發(fā),累計研發(fā)投入超400億元,已在國內(nèi)獲批上市17款創(chuàng)新藥、4款2類新藥,另有90多個自主創(chuàng)新產(chǎn)品正在臨床開發(fā),300余項臨床試驗在國內(nèi)外開展。
除了深耕傳統(tǒng)優(yōu)勢的腫瘤領(lǐng)域,公司還積極開辟新賽道,在代謝性疾病、自身免疫疾病、呼吸系統(tǒng)疾病、神經(jīng)系統(tǒng)疾病、心血管疾病、感染疾病、血液疾病、疼痛管理、眼科等多個領(lǐng)域進行廣泛布局。在自身免疫領(lǐng)域,經(jīng)過多年的沉淀和布局,公司已有10余款產(chǎn)品在研。除中重度斑塊狀銀屑病外,夫那奇珠單抗目前還開展了銀屑病關(guān)節(jié)炎、成人活動性強直性脊柱炎等臨床研究,其中成人活動性強直性脊柱炎已進入上市申報階段。
未來,恒瑞醫(yī)藥將繼續(xù)立足民生需求,爭分奪秒推進創(chuàng)新藥研發(fā),努力研制出更多的新藥好藥,服務(wù)健康中國,惠及全球患者。
關(guān)于SHR-1314-301
SHR-1314-301研究是一項在全國開展的多中心、隨機、雙盲、平行、安慰劑對照的臨床III期研究,旨在對夫那奇珠單抗的有效性和安全性進行評估,共納入690例成人中重度斑塊狀銀屑病患者,隨機按2:1分成夫那奇珠單抗組(240mg Q2W*3+240mg Q4W)和安慰劑組(12周時轉(zhuǎn)為夫那奇珠單抗240mg治療,每2周一次,即第12周、14周和16周連續(xù)3次給藥,之后每4周給藥一次)8。主要研究終點為12周PASI 90的受試者比例以及第12周達(dá)到靜態(tài)醫(yī)師全面評估(sPGA)0/1的受試者比例(sPGA 0/1應(yīng)答被定義為sPGA評分為0[清除]或1[幾乎清除])。關(guān)鍵次要研究終點包括第12周PASI 75/PASI 100的受試者比例、sPGA 0的受試者比例等。研究結(jié)果顯示:
· 夫那奇珠單抗完全清除率高
夫那奇珠單抗組第12周PASI 75應(yīng)答率達(dá)93.6%;PASI 90應(yīng)答率為76.8%(圖1),PASI 90應(yīng)答中位時間僅8.3周(95%CI, 8.1-8.3周),sPGA 0/1應(yīng)答率為71.8%(圖2),均顯著高于安慰劑組。在皮損完全清除方面,夫那奇珠單抗也展現(xiàn)了突出的優(yōu)勢,第12周PASI 100應(yīng)答率達(dá)到36.6%,sPGA 0應(yīng)答率為38.2%,同樣都顯著高于安慰劑組。
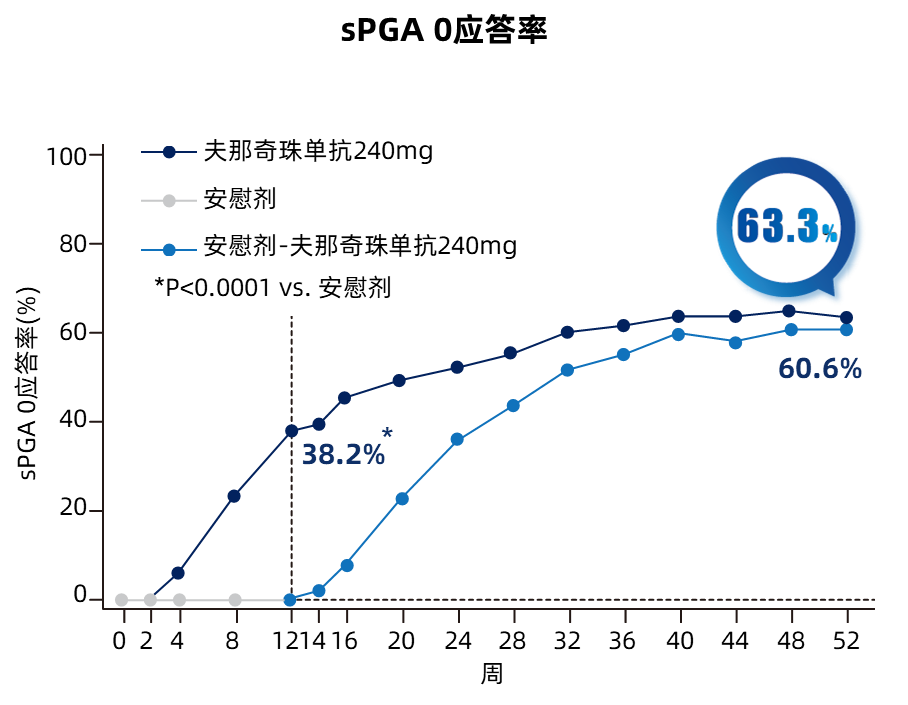
圖1 核心期各次訪視PASI 90應(yīng)答情況趨勢圖

圖2 核心期各次訪視sPGA 0/1應(yīng)答情況趨勢圖
第52周,夫那奇珠單抗組PASI 100應(yīng)答率達(dá)到63.1%(圖3),sPGA 0應(yīng)答率為63.3%(圖4),轉(zhuǎn)換組分別為61.1%和60.6%。

圖3 治療期(核心期+維持期)各次訪視PASI 100 應(yīng)答情況趨勢圖

圖4 治療期(核心期+維持期)各次訪視sPGA 0 應(yīng)答情況趨勢圖
· 夫那奇珠單抗皮損清除起效快
夫那奇珠單抗組在12周內(nèi)PASI評分較基線變化隨時間推移呈明顯下降趨勢,PASI評分較基線的下降百分比均值在第2周時已達(dá)50%以上。根據(jù)Kaplan-Meier法估算,夫那奇珠單抗組核心期達(dá)到PASI 75的應(yīng)答中位時間僅4.3周(95%CI, 4.1-4.4周),安慰劑組未達(dá)。總體來看,第12周之后,夫那奇珠單抗組PASI評分較基線的百分比均值下降趨于平緩,第28-52周均可維持在97%以上。
· 夫那奇珠單抗可提高患者用藥依從性
安全性方面,夫那奇珠單抗組核心期不良事件發(fā)生率與安慰劑組相似,且感染發(fā)生率低,無受試者因為注射部位反應(yīng)而停止治療或終止研究。此外,夫那奇珠單抗密集期僅需注射3次,全年注射14次9,注射便捷性高。
參考文獻(xiàn):
1.中華醫(yī)學(xué)會皮膚性病學(xué)分會銀屑病專業(yè)委員會. 中國銀屑病診療指南(2023版)[J]. 中華皮膚科雜志,2023,56(7):573-625.
2.中華醫(yī)學(xué)會,中華醫(yī)學(xué)會雜志社,中華醫(yī)學(xué)會皮膚性病學(xué)分會,等. 銀屑病基層診療指南(2022年)[J]. 中華全科醫(yī)師雜志,2022,21(8):705-714.
3.Chen K, et al. Clinic characteristics of psoriasis in China: a nationwide survey in over 12000 patients[J]. Oncotarget. 2017;8(28):46381-46389.
4.Menter A, et al. Interleukin-17 and interleukin-23: a narrative review of mechanisms of action in psoriasis and associated comorbidities[J]. Dermatology and Therapy. 2021;11: 385-400.
5.Zhang C, et al. A multicenter, randomized, double-blinded, placebo-controlled, dose-ranging study evaluating the efficacy and safety of vunakizumab in patients with moderate-to-severe plaque psoriasis[J]. J Am Acad Dermatol. 2022;87(1):95-102.
6.張琪,劉保國,李晨昊. IL-17A抑制劑治療銀屑病研究進展[J]. 世界最新醫(yī)學(xué)信息文摘(連續(xù)型電子期刊),2021,21(8):131-134,138.
7.Data on file.
8.Xu Jinhua et al. Efficacy and safety of vunakizumab in moderate-to-severe chronic plaque psoriasis: a randomized, double-blind, placebo-controlled phase 3 trial. EADV 2023.
9.夫那奇珠單抗說明書.
300多萬優(yōu)質(zhì)簡歷
17年行業(yè)積淀
2萬多家合作名企業(yè)

微信掃一掃 使用小程序
